M. Sc. Kevin Hares
Kontakt durchs Sekretariat:
monika.boschtu-dortmundde

Lebenslauf
Kevin Hares begann im Oktober 2013 sein Chemiestudium an der TU Dortmund und schloss seine Bachelorarbeit mit dem Thema "Entwicklung einer tandemkatalytischen Umsetzung von Butadien zu C10-ungesättigten Estern" im Jahr 2016 ab.
Er setzte den Master an der TU Dortmund fort, ging aber im September 2017 nach Großbritannien und studierte über das Erasmus+ Austauschprogramm für 9 Monate am University College London. Am UCL absolvierte er ein Forschungsprojekt mit dem Thema "Kinetic Studies on SSZ-13 and Synthesis of Hierarchical SSZ-13 using Chitosan as Macro-Template". Während dieser Zeit und noch bis März 2019 erhielt Kevin das Deutschlandstipendium der BASF SE.
2019 schloss er seinen Master mit einer Arbeit zum Thema "The Palladium Catalyzed Carboxytelomerization of 1,3-Butadiene with Carboxylic Acids - An Atom Economic Route Towards Mixed Anhydrides" am Lehrstuhl für Technische Chemie (TC) ab.
Seit April 2019 ist Kevin als wissenschaftlicher Mitarbeiter am Lehrstuhl für Technische Chemie tätig.
Forschungsthema
Die moderne chemische Industrie benötigt nachhaltige Umwandlungen von Ausgangsstoffen, die kosteneffizienter und weniger umweltschädlich sein sollen. Ein neuartiger Ansatz hierfür ist die Verwendung von Katalysatoren, die die Aktivierungsenergie eines bestimmten Reaktionswegs senken und somit zu hochselektiven und aktiven Reaktionssystemen führen können.
Einige Reaktionen, die ähnliche Katalysatoren und Reaktionsbedingungen erfordern, können gleichzeitig in einem einzigen Reaktor durchgeführt werden. Wenn derselbe Katalysator diese Reaktionen katalysiert, spricht man von Tandemkatalyse, wie in Abbildung 1 dargestellt.
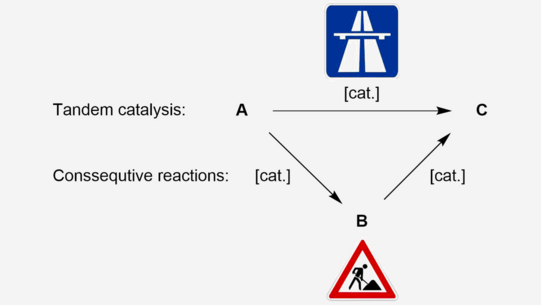
Herkömmliche aufeinanderfolgende Reaktionen erfordern mehrere Schritte und häufig eine Aufarbeitung zwischen den einzelnen Schritten. Diese erfordern Energie und andere Ressourcen, die bei tandemkatalysierten Reaktionen eingespart werden können, da das Reaktionssystem in diesem Fall in der Lage ist, A in einem Reaktionsaufbau direkt in C umzuwandeln (Abbildung 1). Diese "Fast Track"-Route spart also Energie, Zeit und Ressourcen.
Aminierungsreaktionen und Entwurf von Katalysatoren
Die Synthese von Aminen und insbesondere von primären Aminen ist nach wie vor eine Herausforderung und Gegenstand aktueller Forschung. Ein bekannter Weg zu Aminen ist die Aminierung von Alkoholen. Die Selektivität dieser Reaktion ist jedoch schwer zu kontrollieren, da die entstehenden nicht-tertiären Amine unerwünschte Folgereaktionen eingehen können.
Ein neuer Weg für die Synthese von Aminen wäre die Aminierung von Estern, da diese leicht verfügbar sind. Außerdem können Ester aus erneuerbaren Quellen wie Pflanzenöl gewonnen werden, so dass dieser Weg auf einem erneuerbaren Ausgangsstoff basieren kann. Dieser Reaktionsaufbau kann in zwei Schritten oder tandemkatalysiert durchgeführt werden, wie in Abbildung 2 dargestellt.
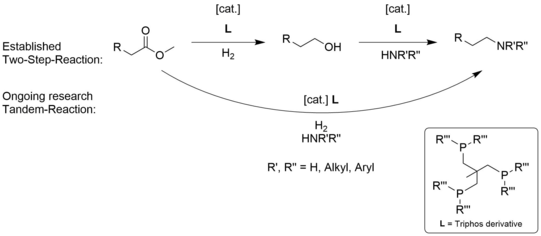
Der Mechanismus dieser Reaktion ist nicht im Detail bekannt, daher ist es von Interesse, die wichtigsten Reaktionsschritte und Zwischenprodukte zu bestimmen. Dies kann durch Variation des Katalysatorsystems erreicht werden. Darüber hinaus können maßgeschneiderte Liganden die Produktivität des Systems erhöhen oder seine Selektivität optimieren. Maßgeschneiderte Liganden sind jedoch in den meisten Fällen nicht kommerziell verfügbar und müssen synthetisiert werden, was ein wichtiger Teil dieser Forschung ist.
Carboxytelomerisierung - ein nützliches Werkzeug in der Synthese
Die Carboxytelomerisierung ist ein weiteres Beispiel für eine äußerst wirtschaftliche tandemkatalysierte Reaktion (Abbildung 3). Sie ist in der Lage, basisches Ausgangsmaterial in wertvolle ungesättigte Produkte, wie ungesättigte Ester, umzuwandeln. Die Reaktion ist unter Verwendung von Alkoholen als Ausgangsmaterial wie Methanol gut bekannt. Jüngste Studien haben jedoch gezeigt, wie flexibel die Reaktion ist.

So war es beispielsweise möglich, Amine und verzweigte Diene in ihre entsprechenden Ester und Amide umzuwandeln (Abbildung 4). Der Umfang der Reaktion kann noch diversifiziert werden und zu neuen wertvollen Produkten führen, um die Synthese-Werkzeug-Carboxytelomerisierung effizient zu erweitern.

Publikationen & Konferenzen
- Hares, K., Wegener, H. W., Roth, T. F. H., Reichert, R., Vogt, D., Seidensticker, T., (2024) "Primary amines from alkenes and carbonyl compounds: highly selective hydrogenation of oximes using a homogeneous Ru-catalyst" Catal. Sci. Technol., Advance Article, DOI: 10.1039/D4CY00368C.
- Hares, K., Vogelsang, D., Wernsdörfer, C.S., Panke, D., Vogt, D., Seidensticker, T. (2022). „Palladium-catalyzed synthesis of mixed anhydrides via carbonylative telomerization” Catal. Sci. Technol., 12, 3992-4000, DOI: 10.1039/D2CY00486K .
- Vogelsang, D. , Vondran, J. , Hares, K. , Schäfer, K. , Seidensticker, T. , Vorholt, A. J. (2019). "Palladium Catalysed Acid-Free Carboxytelomerisation of 1,3-Butadiene with Alcohols Accessing Pelargonic Acid Derivatives Including Triglycerides under Selectivity Control". Adv. Synth. Catal. 362 (3), 679-687, DOI: 10.1002/adsc.201901383.
- Vogelsang, D. , Raumann, B. A. , Hares, K. , Vorholt, A. J. (2017). "From Carboxytelomerization of 1,3‐Butadiene to Linear α,ω‐C10‐Diester Combinatoric Approaches for an Efficient Synthetic Route". Chem. Eur. J. 24 (9), 2264-2269, DOI: 10.1002/chem.201705381.
- März 2021, Weimar, Germany, 54. Jahrestreffen Deutscher Katalytiker, "Expanding the synthesis tool carboxytelomerization-More efficient amide synthesis and new products"




